4- Infection du pied diabétique
4- Infection du pied diabétique :
4.1- Définition :
C’est une invasion des tissus par des microorganismes et leur multiplication s’accompagnant d’une destruction tissulaire ou d’une réponse inflammatoire de l’hôte.
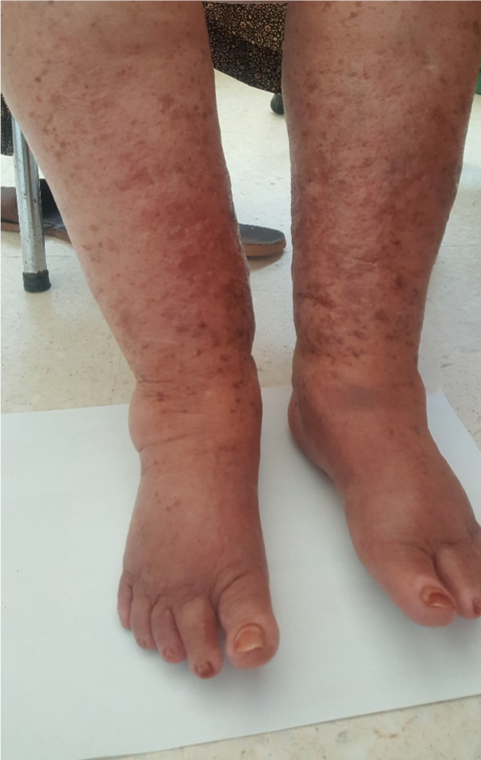
Le diagnostic se base sur la présence d’au moins deux signes de l’inflammation : Œdème, érythème, douleur, chaleur et induration ou par la présence de pus au niveau de l’ulcération.
La fréquence des infections est expliquée par un déficit des défenses cellulaires avec de nombreuses anomalies des polynucléaires aggravées par une hyperglycémie.
Les infections superficielles : Elles ne mettent pas en danger les membres inférieurs, elles touchent la peau et les tissus sous cutanés sans atteindre les structures plus profondes. C’est une cellulite sans lymphangite ou abcès. Elles sont mono-bactériennes en général, le plus souvent à Cocci à Gram positif en particulier le staphylocoque doré (17,18).
La Dermo-Hypodermite Bactérienne (DHB) : Elle est l’atteinte de l’hypoderme avec des signes locaux de rougeur péri- lésionnelle puis diffuse.
Photo 5
Les infections modérées ou sévères : Elles atteignent les tissus profonds (fascia, articulation et os), sont souvent poly-microbiennes à Cocci à Gram positif, à Gram négatif et anaérobies.
Elles sont la cause directe de 25 à 50% des amputations chez le diabétique (19, 20,21). Ce sont des abcès profonds, une cellulite extensive, un phlegmon des gaines ou une septicémie. Malgré la sévérité, l’hyperleucocytose et la fièvre peuvent manquer, leur présence est un signe de gravité. Le déséquilibre glycémique peut être le seul signe d’alerte(19).
La Dermo-Hypodermite Bactérienne Nécrosante ou Fasciite Nécrosante (DHBN-FN) : C’est une nécrose tissulaire de l’hypoderme et du derme. Elle se manifeste par un décollement cutané et une coloration violacée de la peau sans pus ni abcès, on notera une altération de l’état général et une insuffisance rénale.
La gangrène humide est définie par une nécrose tissulaire noirâtre, rapidement évolutive associée à un décollement et un pus nauséabond grisâtre avec sepsis et déséquilibre métabolique.
4.2- Evaluation de la plaie : Nature, classification, stade évolutif
4.2.1- Nature :
Différencier les plaies neuropathiques des plaies ischémiques ou mixtes (20).
Voir tableau 3 joint.
4.2.2- Classifications des plaies du pied diabétique (21,22).
Elle doit être réalisée chez tout diabétique une fois par an. Elle permet de définir le grade du risque lésionnel et d’orienter le patient sur une prise en charge spécifique. Plusieurs classifications sont disponibles dans la littérature internationale.
La première étant celle de Wagner : Elle est cotée de 1 à 5 selon la profondeur de l’ulcère, la présence d’infection ou de gangrène.
Classification SAD : Acronyme de sepsis, artériopathie, dénervation, Size (Profondeur et surface).
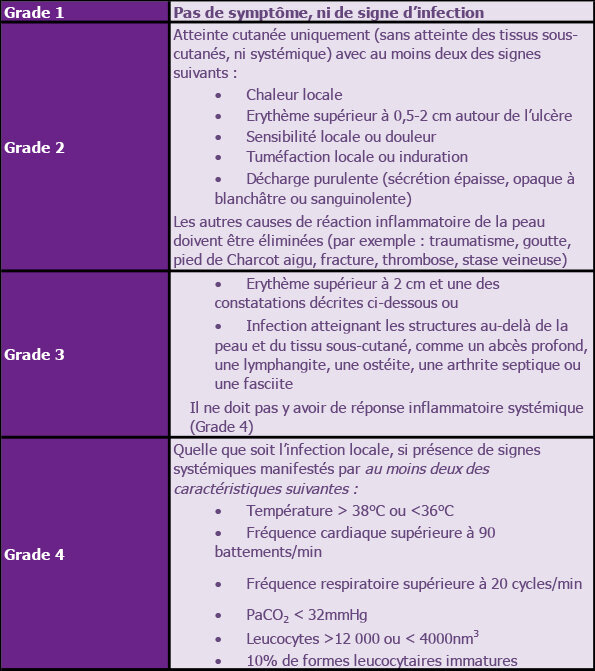
Classification de l’infection des plaies du pied selon le Consensus International sur le pied diabétique.
Classification UT de l’université du Texas. Elle a combiné la profondeur de l’atteinte en 4 grades et la présence ou non de l’infection et/ou une ischémie en 4 niveaux.
Voir Tableaux joints.
Tableau 3 : Symptômes cliniques des ulcères du pied neuropathiques et ischémiques(20).
Tableau 4 : Classification de la sévérité de l’infection selon le consensus international sur le pied diabétique(24).
Tableau 5 : Classification de l’université de Texas(23).
4.2.3- Stade évolutif :
L’infection du pied diabétique doit être diagnostiquée cliniquement sur la base de signes locaux ou systémiques ou de symptômes d’inflammation (15). C’est une infection des parties molles secondaire à une plaie du pied. Ultérieurement, une ostéite peut survenir par contiguïté.
Pour établir la gravité de l’infection du pied diabétique, il faut évaluer les signes généraux, la biologie et la gravité par un débridement de la plaie. Pour le diagnostic d’infection osseuse, recourir à l’imagerie ; la radiographie standard en premier et si nécessaire l’IRM ou le PET-scan(7).
Ne pas méconnaitre les urgences chirurgicales. Un débridement chirurgical large en cas de dermo-hypodermite bactérienne ou fasciite nécrosante est nécessaire.
4.3- Détersion nettoyage de la plaie :
La détersion a pour but d'éliminer les tissus dévitalisés et/ou infectés, les débris et corps étrangers emprisonnés dans la plaie, la kératose entourant la plaie pour mettre à nu le tissu sain. La présence de tissu nécrotique retarde la cicatrisation et augmente le risque d'infection. Les tissus à déterger peuvent se présenter sous l'aspect de plaques nécrotiques noirâtres et/ou d'une masse jaunâtre, ferme et adhérente, appelée fibrine.
4.3.1- Le débridement mécanique :
Au bistouri, scalpel ou curette en salle de soins ou au bloc opératoire, par un opérateur expérimenté. Il consiste à exciser les parties molles nécrosées, les tissus dévitalisés et contaminés et le tissu fibreux.
Avant tout geste de débridement, il faut rechercher une artériopathie. Autant dans les ulcérations à prédominance neuropathique, le débridement doit être appuyé jusqu'à parvenir au tissu sain, autant dans les ulcères ischémiques, il doit être très prudent et se limiter à un simple drainage.
L’idéal est de débrider après ou lors de la revascularisation. Il est contre indiqué s’il y a un traitement anticoagulant.
Ce débridement permet un meilleur drainage des exsudats et la réalisation de prélèvements bactériologiques profonds. Il doit toujours précéder l’application de tout agent topique et doit être répété aussi souvent que nécessaire.
4.3.2- La Détersion auto lytique : Action de phagocytose, des macrophages et sécrétion d’enzymes protéolytiques, favorisée par un microclimat humide.
4.3.3- La Détersion chimique : Par Dakin ou eau oxygénée, reste exceptionnelle, il faut éviter les produits agressifs. Le lavage de la plaie au sérum physiologique en jet à la seringue reste la règle pour maintenir un certain degré d’humidité de la plaie.
4.4- Traitement général et local :
Il comprend des mesures générales et locales.
4.4.1- Le traitement général vise à :
Obtenir un équilibre glycémique optimal par une insulinothérapie pluriquotidienne, le plus souvent pour accélérer le processus de cicatrisation et ralentir l'évolution de la neuropathie
Lutter contre une éventuelle infection par une antibiothérapie générale : Rappeler que le diagnostic reste clinique et que les examens bactériologiques ne sont pas indiqués en l'absence de suspicion clinique d'infection. Ne pas traiter par antibiothérapie une plaie cliniquement non infectée pour prévenir l'apparition hypothétique d'une infection.
Restaurer un bon apport artériel en présence d'une artériopathie des membres inférieurs par des techniques de pontages distaux fiables. Les angioplasties prennent une place de plus en plus importante dans les gestes de revascularisation. Les traitements vaso-actifs (les prostacyclines et les prostanoïdes) n’ont pas prouvé leur efficacité en raison du mauvais état cardio-vasculaire de ces patients.
Prévenir les thromboses dues à l'alitement et/ou l'infection, par injection d'héparine de bas poids moléculaire qui pourrait augmenter le taux de cicatrisation des ulcères ischémiques et diminuer le taux d’amputations'(22,23).
Résorber l'œdème qui ralentit par effet "mécanique" la cicatrisation.
Assurer un apport nutritionnel adéquat, la malnutrition augmente en effet le risque de retard de cicatrisation et d’infection.
Calmer la douleur. Les douleurs neuropathiques des membres inférieurs (forme hyperalgique) associent paresthésies, allodynies et hyperalgésie contrastant avec l'indolence de la plaie. La Food and Drug Administration des États-Unis (FDA) a approuvé trois médicaments la prégabaline, la duloxetine et le tapentadol, pour le traitement de la douleur associée à la neuropathie périphérique diabétique mais aucun ne procure un soulagement complet même lorsqu’il est utilisé en association. On utilisera les antidépresseurs tricycliques tel que (amitriptyline) à une dose de 25 mg à 150 mg; c'est un médicament accessible sur le plan financier, disponible au niveau des hôpitaux et très efficace sur les douleurs neuropathique.
Les antalgiques paliers I et II, les antiépileptiques (carbamazépine), les opioïdes et opiacés, (tramadol), la prégabaline, et la gabapentine, sont autant de molécules utilisées dans la littérature internationale, mais aucun ne procure un soulagement complet de la douleur, même lorsqu'il est utilisé en association.
Vérifier le statut vaccinal antitétanique.
4.4.2- Le traitement local :
Il comprend la mise en décharge de la plaie, sa détersion, son nettoyage et son recouvrement.
4.5- Quels Pansements choisir:
Le pansement idéal crée un microclimat humide, perméable aux échanges gazeux favorisant la cicatrisation. Il enlève l’excès d’exsudat et les composants toxiques, augmente la température au niveau de la plaie. Il doit être stérile et non adhérent à la plaie. Le choix dépend :
1- Du stade de cicatrisation ; qui suit les étapes suivantes :
Phase exsudative
Phase de bourgeonnement : Apparition de tissu de granulation
Phase de réépidermisation ou épithélialisation : Le tissu de granulation devient tissu de cicatrisation.
2- De l’aspect de la plaie :
Mettre un pansement neutre visant à contrôler l'exsudat et à maintenir un milieu humide.
Les pansements à base de nitrate d’argent sont indiqués en cas de lésions superficielles (19).
Par analogie avec les autres plaies chroniques, les bénéfices d'un microclimat humide dans la plaie du pied diabétique, sont actuellement reconnus à toutes les étapes du processus de cicatrisation (24).
Tableau 6: Choix du pansement en fonction de la plaie (24)
4.6- Quand prescrire une antibiothérapie?
L'antibiothérapie n'est pas systématique. Elle dépend de l'aspect de la plaie et de l'état général du patient. Nous recommandons ce qui suit:
Plaies sans signes inflammatoires ni écoulement : Pas d’antibiotiques.
Plaies et signes inflammatoires : Attendre le résultat des prélèvements.
Plaies avec signes généraux et signes locaux d’infection : Antibiothérapie empirique
Ostéite chronique : Attendre les prélèvements (24,25).
Traiter d’emblée par antibiothérapie en présence de l'un des signes suivants (9,21):
Devant une douleur ou ulcération associée à une porte d’entrée infectée ou un défaut de cicatrisation.
Devant une fièvre dans les formes sévères.
Devant la présence d'un contact osseux.
Devant une gangrène humide, il faut prescrire une antibiothérapie ciblant les anaérobies.
Dans tous les autres cas, confirmer l’infection avant l’antibiothérapie par des prélèvements bactériologiques. Les germes responsables étant variables selon le type de plaie et la durée de son évolution, la consultation des recommandations thérapeutiques est nécessaire pour une aide au diagnostic.
Tableau 7 : Corrélation clinico-bactériologique selon le type de plaie [37]
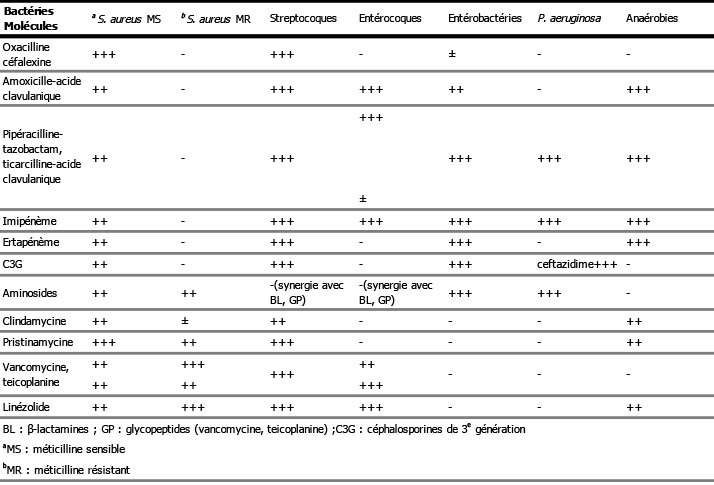
Tableau 8 : Spectre d’activité des principaux antibiotiques utiles dans les infections du pied diabétique (hormis les ostéites) [22].
4.7- Rechercher une ostéite
L'infection de l’os ou de l’articulation se fait le plus souvent par contiguïté à partir d’une plaie. Elle est présente dans 30 à 80% des cas selon la gravité chez le diabétique.
4.7.1- Diagnostic
On doit l'évoquer devant plusieurs situations cliniques:
En cas de résistance au traitement, récidive de l’infection ou d’une ulcération surtout lorsqu’elle siège en regard d’une proéminence osseuse.
En cas d’évolution défavorable ou trainante malgré une prise en charge optimale.
En cas de contact osseux rugueux au moyen d’une sonde métallique stérile à pointe mousse introduite à travers l’ulcération.
En cas d’exposition osseuse avec aspect érythémateux, œdématié en saucisse d’un orteil ou une mobilité anormale de celui-ci.
Le diagnostic différentiel se pose avec le pied de CHARCOT aigu. L’absence de neuropathie et d’une artériopathie sévère plaide en faveur d’une ostéo-arthrite.
La radiographie standard est peu contributive ; la réaction périostée, l’ostéolyse ou l’ostéopénie ne sont évidents qu’après destruction de l’os.
L’IRM est l’examen radiologique de choix. La scintigraphie aux polynucléaires marqués aide au diagnostic, mais la biopsie osseuse est l’élément clé pour le diagnostic bactériologique d’ostéite.
4.7.2-Quelle antibiothérapie en cas d’ostéite ?
Le choix des antibiotiques sera fait selon leur spectre et leur diffusion osseuse. En effet, en se basant sur les critères suscités pour la suspicion des bactéries, le choix du traitement de première intention sera fait puis adapté à l'antibiogramme de l'isolat microbiologique.
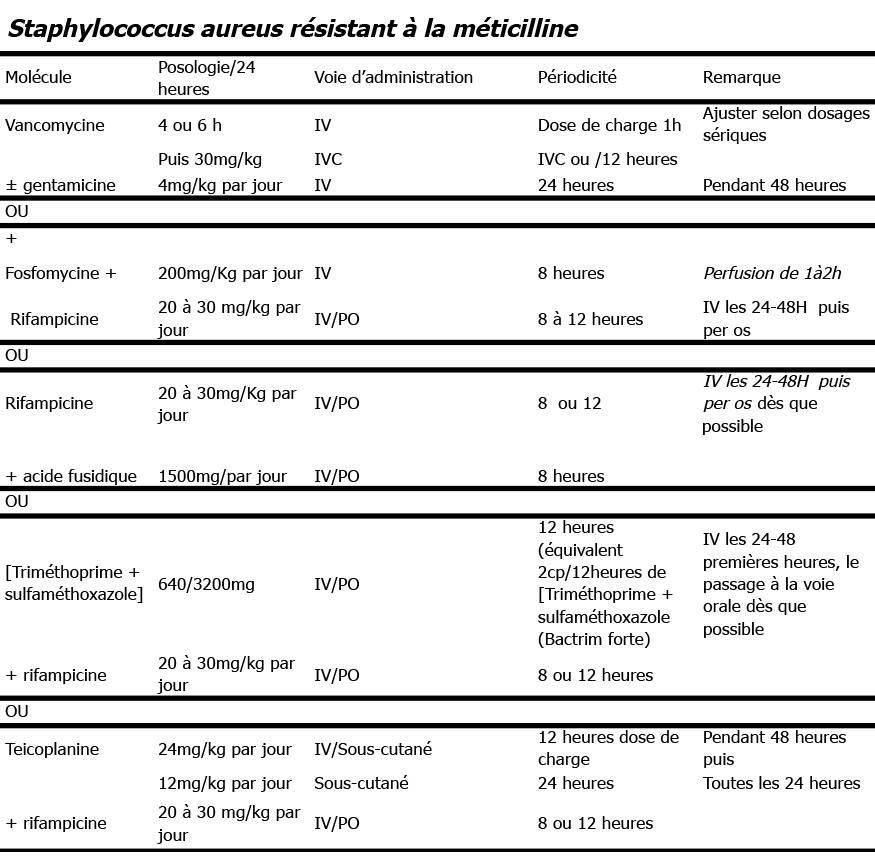
Le consensus français de 2009 nous propose plusieurs traitements de première intention détaillés sur les tableaux suivants (22).
Tableau 9: Recommandations pour le choix de l’antibiothérapie lors d'ostéite aigüe du pied chez le diabétique [40]
4.7.3- Principes de l’antibiothérapie en cas d’ostéite :
Antibiotiques à bonne diffusion osseuse. A doses maximales, si présence d’une ischémie.
Recourir aux molécules suivantes : Linézolide et Ertapenem s’il y a des multi résistances.
Une réévaluation est à effectuer après 48 à 72 heures. Si elle est favorable, il faut garder la même antibiothérapie.
Adapter l’antibiothérapie à la culture si l’évolution est défavorable et rechercher une cause de l’échec comme une inobservance au traitement, l’absence de décharge ou une extension de l’ischémie.
Tenir compte de l’insuffisance rénale ou cardiaque ou d’une gastroparésie chez le diabétique(26,27).
4.8- Quand hospitaliser ?
Infection sévère et une mauvaise compliance du patient avec mise en jeu du pronostic vital.
Plaie profonde et atteinte ostéo articulaire probable.
Evolution rapide et défavorable de la plaie.
Déséquilibre glycémique.
Ischémie sévère ou gangrène.
Nécessité d’une antibiothérapie intraveineuse non réalisable à domicile.
Nécessité d’un geste chirurgical.
Impossibilité de soins ou de suivi.
4.9- Durée de l'antibiothérapie
Pour une infection légère ou modérée des parties molles, 15 jours d’antibiothérapie suffisent (19). Pour une ostéite avérée, prescrire 6 semaines d’antibiothérapie à diffusion osseuse quand aucune résection osseuse n’est pratiquée.
Dans les situations où une résection osseuse large de l’os infecté a été réalisée, une semaine d’antibiothérapie est préconisée.
4.10- Facteurs de croissance :
Sont regroupés sous ce terme un grand nombre de polypeptides impliqués non seulement dans les phénomènes de la croissance cellulaire, mais aussi dans les processus physiologiques de la cicatrisation (2).
Parmi les nombreux facteurs de croissance identifiés jusqu'à maintenant, le PDGF, le FGF, les TGF-alpha et -beta, ainsi que l'EGF et les substituts cutanés (Dermagraft) jouent le rôle le plus important dans la réparation cutanée dans les ulcères neuropathiques du pied diabétique (28,29).
4.11- Gel autologue d’agrégat plaquettaire ou PRP :
Après centrifugation du sang du patient, le médecin recueille le PRP qu'il applique stérilement sur la zone à cicatriser. Cette couche de PRP améliore la durée et la qualité de la cicatrisation (30).
4.12- Vacthérapie :
Permet un drainage des exsudats et des agents inhibiteurs de la cicatrisation, augmente le flux sanguin local, diminue l’œdème tissulaire avec formation de tissu bourgeonnant.
On utilise une mousse multi pores, un film adhésif et un drainage par pression négative (-125 mm Hg) continue ou discontinue. Il y a un changement de réservoir tous les 3 à 5 jours, une déconnexion de l’unité 2 heures par jour sur une durée totale de 22 jours en moyenne.
On arrête la Vacthérapie s’il y a apparition de tissu de bourgeonnement ou si douleur persistante non améliorée après 2 pansements et en cas d’infection ou de saignement. La pose se fait au bloc opératoire sous anesthésie générale.
4.13- Oxygénothérapie hyperbare (27,31)
Le recours au caisson hyperbare ou à la thérapie par pression négative (TPN) peut être envisagé dans les plaies post-opératoires après amputation.
Une amélioration à court terme peut être envisagée avec une pression de 2 à 2,5 ATA et une durée d’inhalation de 90 à 120 minutes, une à deux fois par jour pendant 10 séances. Elle a un effet rhéologique et une action sur l’ostéogenèse.